La química es una ciencia que se ha servido para dar explicación a los fenómenos que ocurren en la naturaleza, en relación a los procesos químicos que la afectan. Son muchos factores los que inciden sobre la materia para que esta sufra cambios, ya se hagan dentro o fuera de un laboratorio. Así mismo, siempre trabaja de la mano de la física para dar con las respuestas adecuadas. El principio de Chatelier o Le Chatelier, también conocido como el principio del equilibrio químico, es uno de los postulados que plantea como a pesar de que un sistema sufra cambias, su equilibro químico se mantendrá. Y es que a pesar de que ciertos factores interfieran, se presentará una evolución para seguir manteniendo dicho equilibrio.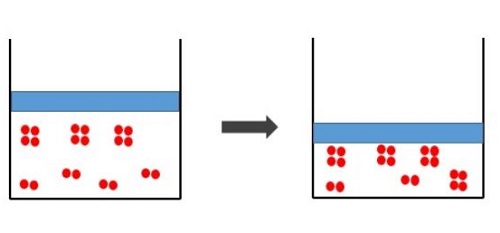
Esta fue una teoría presentada por el químico industrial Henri-Louis Le Chatelier. Y en su definición explica como el sistema evoluciona, y se ve beneficiado por un catalizador que permite que el proceso se acelere. Se tiene en cuenta que, este elemento no interfiere en ningún momento dentro del proceso de lograr el equilibrio químico. Este simplemente permite que sea más rápido alcanzarlo.
Qué es el principio de Chatelier
En 1884, Henri-Louis Le Chatelier, un químico industrial de origen francés establece la definición del equilibrio químico, estudiando los factores que posiblemente pueden afectar un sistema. Este fue nombrado como el principio de Chatelier, en honor a su autor.
Es de esta manera, que se define que cuando un sistema se ve afectado por algún factor externo, entonces este evolucionará y encontrará la manera de ajustarse para no verse perturbado, y poder alcanzar un nuevo equilibrio. De aquí nace el término equilibrio químico, el cual se logra al evitar que el cambio de condiciones perjudique la integridad de un sistema.
También, a través de este enunciado, se determinó la existencia de algunos parámetros que pueden modificarse y afectar el equilibrio. En estos se encuentra: la temperatura, la presión y la concentración. En el momento en que se presente una variación, entonces el sistema buscará como ajustarse para que los efectos no sean perjudiciales. Y de esta manera se considera que es capaz de alcanzar un nuevo equilibrio químico, evolucionando y manteniendo su integridad.
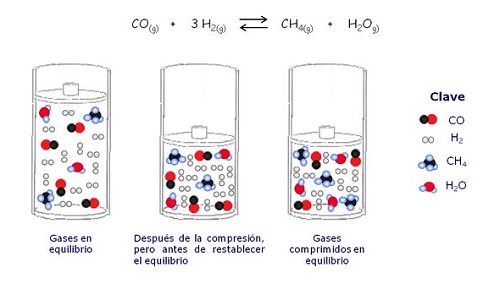
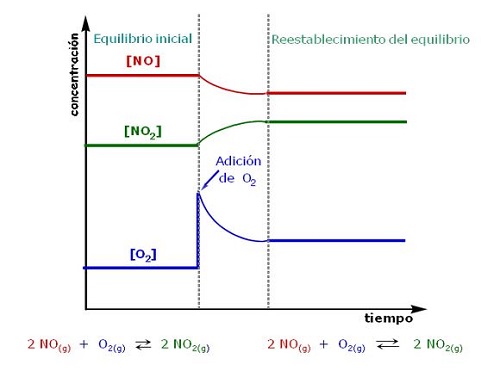
Principio de Chatelier sobre el efecto de la concentración
Cuando se habla de concentración, se tiene que si existe una variación sobre esta, entonces existe la posibilidad de que el equilibrio químico se vea afectado. Según lo expuesto por Le Chatelier, teniendo en cuenta los experimentos realizados, deduce que la concentración se puede considerar como una fuerza dentro de los componentes del sistema.
Supongamos que se añade H2: H2 (g) + I2 (g) ⇄ 2 HI(g) . El sistema, que hasta el momento ha permanecido en equilibrio, buscará la manera de lograr que el efecto que ocasiona la adición de este elemento disminuya. Se tiene entonces que, H2 y I2 se combinan, formando de esta manera HI. Para lograr el equilibrio, se presenta un aumento en HI, mientras que I2 disminuye.
Pero si en caso contrario, se presenta la remoción de H2, lo que ocurrirá es que el sistema pasará a descomponer HI, formando un nuevo H2 que pasará a sustituir el que desapareció.
Principio de Chatelier sobre el efecto de la presión
La presión es otro factor que se puede considerar esencial dentro del equilibrio de un sistema. Una ligera variación, y la integridad de este se podría ver afectada. Aun así, cabe la posibilidad de que aunque esta cambie, no se presente ningún efecto sobre el equilibrio. Este se puede explicar de la siguiente manera:
En caso de presentarse un aumento de presión dentro de 2 NO2 (g) ⇄ N2O4 (g), la reacción pasará a formar parte del lado donde el número de moles de gas presentes sea menor. Esto va a regular el aumento de la presión dentro del sistema. Si lo que se observa es una disminución de la presión, lo que ocurre es que la reacción se ubicará en el lado con mayor número de moles de gas para mantener la presión.
Principio de Chatelier sobre el efecto de la temperatura
Cuando se hace mención del factor temperatura, hay que tomar en cuenta dos casos de estudio. Tenemos en primer lugar la presencia de una reacción endotérmica. Esta hace referencia a que en la variación de la temperatura, se presente una elevación, entonces la reacción pasará a formar parte del lado donde sea posible absorber el calor.
En segundo lugar, se presenta una reacción exotérmica. Esta se presenta en los casos en que la variación de la temperatura se asocia a una disminución. Aquí la reacción se traslada al lado donde sea posible el desprendimiento de calor. Es así como el sistema mantendrá el equilibrio químico, tratando de adecuarse a los efectos que se presenten.
Como ejemplo, se tiene la siguiente fórmula: CH2 = CH2 (g) + H2 (g) CH3 – CH3 (g) ΔH= -136 Kj/mol. Esto se trata de un proceso de hidrogenación del etano. Aquí se presencia una reacción exotérmica. En este caso, el equilibrio se alcanza a través del desprendimiento de calor debido a una disminución de calor. La reacción se traslada donde ocurre la producción de etano.
Cuando se trata de la deshidrogenación del etano, donde existe un aumento de temperatura, el sistema para lograr el equilibrio, traslada la reacción al lado donde ocurre la regeneración de etileno e hidrógeno, permitiendo la absorción de calor.
Principio de Chatelier sobre el efecto de la catálisis
Según lo propuesto por el principio de Chatelier, no se toma en cuenta que exista la presencia de un catalizador. Pero esto no es del todo cierto. Si bien el postulado se enfoca en asegurar que un sistema puede permanecer en equilibrio químico a pesar de verse afectado por alguna variación, puede acelerarse este proceso. Es necesario que el catalizador no interfiere en ningún momento con el mantenimiento del equilibrio.
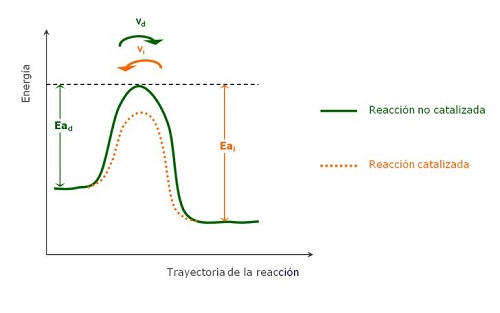
En realidad, este funciona como un acelerador. Cuando en un sistema que se encuentra afectado, hay presencia de un catalizador, este permitirá que el proceso en que es posible devolver el equilibrio sea más rápido. Él forma parte de la reacción que ocurre para lograr tal fin, aunque no existe posibilidad de que este pueda ser capaz de transformarla.